
O iSGLT2 pode reduzir a nefrotoxicidade por cisplatina? Estudo interessante na onconefrologia!
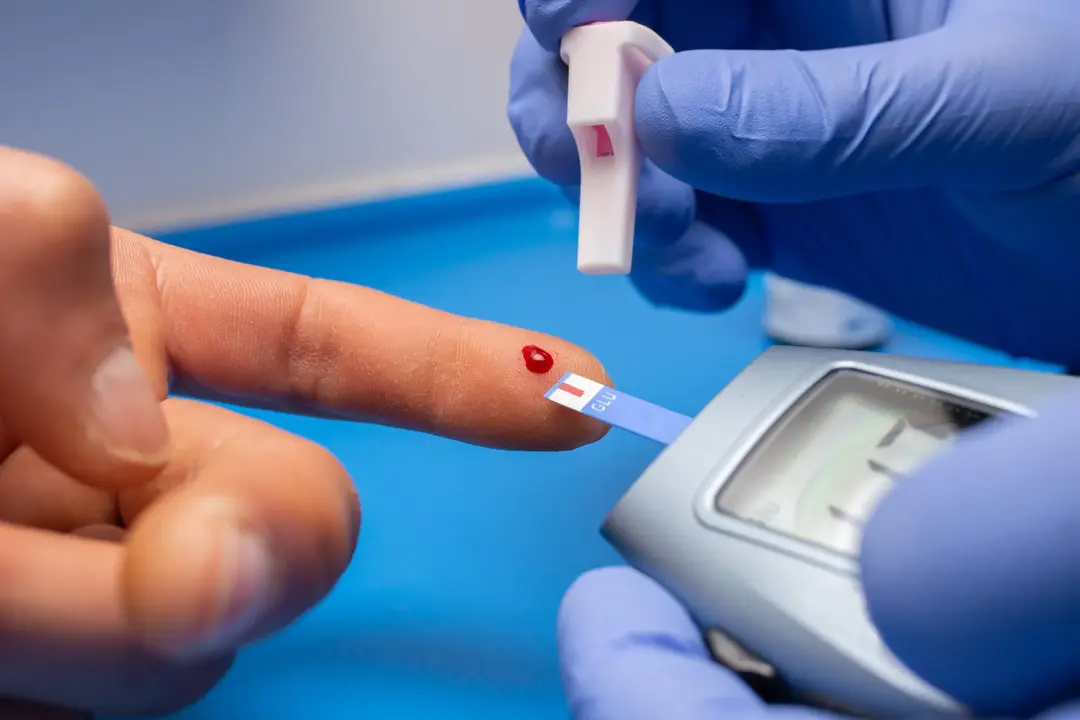
Segurança do uso dos iSGLT2 na DRC

iSGLT2: um coadjuvante no tratamento da anemia relacionada à DRC?
Magnésio na veia antes da quimio pode proteger seu rim da cisplatina!

Infecção urinária durante o uso de iSGLT2: parar ou continuar?
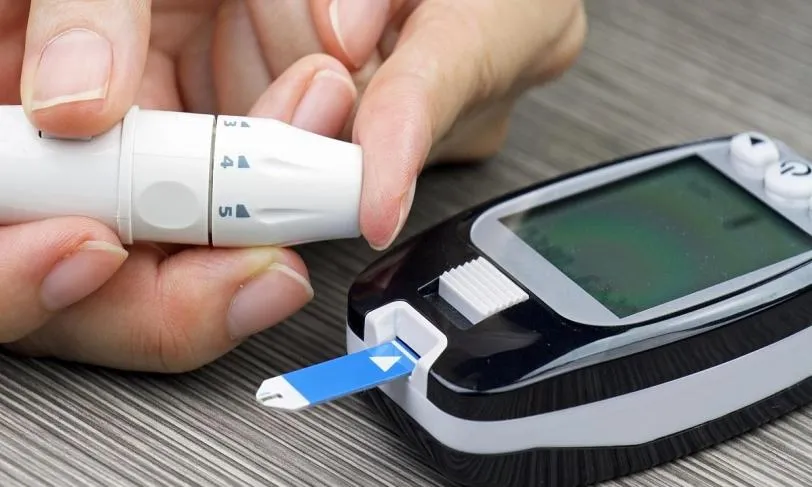
iSGLT2 no perioperatório: risco de cetoacidose e manejo prático Introdução
Empagliflozina para prevenção de cálculos renais em não diabéticos: será que funciona?
**Imagine o seguinte cenário**...
Uma paciente de 66 anos, diabética, hipertensa, com TFGe de 82 mL/min/1,73 m², em uso de metformina, empagliflozina e losartana. Ela foi diagnosticada com carcinoma de cabeça e pescoço e iniciará quimioterapia com cisplatina.
Na discussão com a oncologia, surge aquela pergunta prática: “**Devemos suspender o iSGLT2 antes da cisplatina para evitar desidratação e IRA?** **Ou manter pode até proteger o rim?**”
Durante muito tempo, a resposta intuitiva seria: “melhor suspender tudo que possa mexer com volemia”. Mas esse artigo traz uma provocação interessante: talvez, em pacientes selecionados, o iSGLT2 não seja o vilão — pode ser parte da proteção tubular.
## Qual foi a pergunta do estudo?
Os autores quiseram responder: em pacientes com câncer e diabetes recebendo cisplatina, o uso de inibidores de SGLT2 está associado a menor risco de IRA associada à cisplatina?
Aqui é importante já deixar claro: não foi um estudo randomizado. Foi uma coorte retrospectiva, de centro único, no MD Anderson, usando pareamento por escore de propensão. Ou seja: é um estudo gerador de hipótese, mas com um sinal clínico bem interessante.
## Por que isso faz sentido biologicamente?
A cisplatina é clássica na onconefrologia: eficaz contra vários tumores, mas nefrotóxica. A toxicidade ocorre principalmente por acúmulo da droga nas células tubulares proximais, com estresse oxidativo, inflamação, lesão mitocondrial, apoptose e necrose tubular.
Além da IRA, a cisplatina pode causar:
- Perda renal de magnésio
- Perda de sal
- Diabetes insipidus nefrogênico
- Síndrome de Fanconi
- Queda sustentada da função renal
**E onde entra o iSGLT2?** A hipótese é que os iSGLT2 possam reduzir a captação tubular da cisplatina, modular inflamação, reduzir estresse oxidativo e proteger a mitocôndria tubular. Em modelos animais, canagliflozina e dapagliflozina já haviam mostrado atenuação da lesão tubular induzida por cisplatina. O que faltava era dado clínico em humanos.
## Como o estudo foi feito?
Os autores avaliaram pacientes adultos com câncer, diabetes mellitus e exposição à cisplatina intravenosa entre julho de 2017 e janeiro de 2024. Foram incluídos pacientes que:
- Tinham diabetes
- Usavam medicações antidiabéticas
- Receberam pelo menos uma dose de cisplatina
- Tinham creatinina monitorada após cada dose
- Tinham exposição documentada a iSGLT2, GLP-1RA ou DPP-4i
Depois do pareamento por escore de propensão, ficaram 144 pacientes no grupo iSGLT2 versus 144 pacientes no grupo controle. O grupo iSGLT2 incluía principalmente empagliflozina, dapagliflozina, canagliflozina ou ertugliflozina. A maioria dos pacientes do grupo iSGLT2, cerca de 87,5%, manteve a medicação durante todo o tratamento com cisplatina.
## Qual foi o desfecho principal?
O desfecho principal foi IRA, definida como aumento de pelo menos 50% da creatinina sérica em até 4 semanas após cada infusão de cisplatina. Essa definição é prática e clinicamente relevante, embora não capture todos os detalhes de diurese ou biomarcadores estruturais.
## O que o estudo encontrou?
Aqui vem o dado principal: IRA ocorreu em 13,9% dos pacientes em uso de iSGLT2 versus 28,5% no grupo controle (OR 0,42; IC 95% 0,23–0,76; p = 0,004).
Traduzindo para a prática: neste estudo, o uso de iSGLT2 esteve associado a uma redução importante da chance de IRA associada à cisplatina. E não foi só IRA “qualquer”. O grupo controle teve mais IRA em todos os estágios:
- IRA estágio ≥ 1: 28,5% vs 14%
- IRA estágio ≥ 2: 12,5% vs 8%
- IRA estágio 3: 3,5% vs 1%
Além disso, entre os que desenvolveram IRA, a recuperação renal completa em 3 meses foi numericamente maior no grupo iSGLT2: 65% vs 48,8%.
## E a TFGe depois da cisplatina?
Outro achado interessante: aos 3 meses após a cisplatina, a TFGe média foi maior no grupo iSGLT2 (84,4 vs 78,3 mL/min/1,73 m²; diferença média: 6,08 mL/min/1,73 m²; p = 0,043). Isso sugere que o benefício pode não ser apenas “menos IRA aguda”, mas talvez uma melhor preservação de função renal no curto prazo após o tratamento.
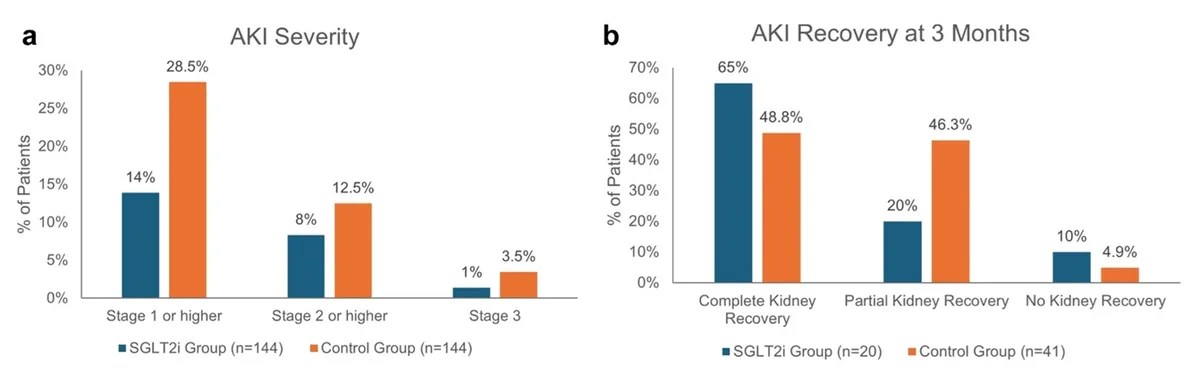
*Figure 1: Gravidade e recuperação da IRA após cisplatina.*
## E o magnésio? Esse ponto é muito importante
A cisplatina causa perda renal de magnésio, e hipomagnesemia é mais do que um “número baixo”: ela pode piorar a nefrotoxicidade da própria cisplatina. Neste estudo, o grupo iSGLT2 teve muito menos hipomagnesemia (23,2% vs 57,3%; OR 0,23; IC 95% 0,14–0,38; p < 0,001).
Esse talvez seja um dos achados mais interessantes para o nefrologista. Por quê? Porque a suplementação de magnésio já é uma das estratégias usadas para reduzir nefrotoxicidade por cisplatina. Se o iSGLT2 também reduz perda renal de magnésio ou melhora o balanço de magnésio, pode haver um mecanismo adicional de proteção.
## Teve impacto em sódio e anemia?
Sim, mas com nuances. A hiponatremia foi numericamente menor no grupo iSGLT2 (60,4% vs 67,4%), mas sem significância estatística. Já a anemia foi menos frequente no grupo iSGLT2 (83,3% vs 95,1%; OR 0,21; IC 95% 0,09–0,52; p < 0,001). Esse achado é biologicamente plausível, já que iSGLT2 pode aumentar eritropoietina e melhorar metabolismo do ferro, mas em pacientes oncológicos isso deve ser interpretado com cuidado.
## Mas foi seguro manter iSGLT2 com cisplatina?
Esse é o ponto que exige individualizar a depender do cenário clínico. Não houve diferença significativa em infecções geniturinárias entre os grupos. Mas houve 2 casos de cetoacidose diabética no grupo iSGLT2 e nenhum no grupo controle.
Isso importa muito. Paciente oncológico em quimioterapia pode ter náuseas, vômitos, baixa ingesta, perda de peso, jejum para procedimentos, infecção, corticoide, desidratação e internações. Tudo isso aumenta o risco de cetoacidose euglicêmica associada ao iSGLT2. Então a mensagem não é: “mantenha iSGLT2 em todo mundo”. A mensagem é: talvez não devamos suspender automaticamente em todos os pacientes estáveis, mas precisamos individualizar e monitorar bem.
## O que este estudo NÃO permite?
Esse ponto é essencial. O estudo não prova causalidade. Também não autoriza iniciar iSGLT2 exclusivamente para proteger o rim da cisplatina, especialmente em pacientes sem diabetes ou em pacientes instáveis. Os próprios autores concluem que os dados são promissores, mas ainda insuficientes para recomendar iniciar iSGLT2 apenas com objetivo de nefroproteção contra cisplatina. Precisamos de ensaio clínico randomizado.
### Opinião NefroAtual
A grande mensagem deste estudo é que o iSGLT2 pode ser mais do que uma medicação cardiometabólica no paciente oncológico diabético. Ele pode ter um papel potencial na proteção tubular durante a exposição à cisplatina. Mas ainda estamos no campo do “sinal promissor”, não da recomendação definitiva.
Na prática, talvez a melhor pergunta não seja mais: “Todo paciente em cisplatina deve suspender iSGLT2?” E sim: “Este paciente específico tem mais risco de complicação com o iSGLT2 ou pode se beneficiar de mantê-lo com monitoramento próximo?”
Você já tinha pensado no iSGLT2 como possível estratégia de proteção renal na cisplatina? Ou ainda suspende automaticamente antes da quimioterapia?
## Referência:
Cintrón-García JJ, Patel M, Andersen CR, et al. Potential Benefit of Sodium-Glucose Cotransporter 2-Inhibitors in Cisplatin-Associated Nephrotoxicity Among Patients With Cancer Having Diabetes Mellitus. Kidney International Reports, 2026.] ([link](https://www.sciencedirect.com/science/article/pii/S2468024926027701))
